医药 · 看点
国务院发布《关于服务“六稳”“六保”进一步做好“放管服”改革有关工作的意见》,允许网络销售部分处方药;《不合理医疗检查专项治理行动工作方案》《基于同类治疗药物的肿瘤伴随诊断试剂说明书更新与技术审查指导原则》《用于产生真实世界证据的真实世界数据指导原则(试行)》等文件发布;财政部发布19家医药企业行政处罚结果……4月12日~18日,医药行业的这些事情值得关注。
行业 · 政策动态
1.国务院发布《关于服务“六稳”“六保”进一步做好“放管服”改革有关工作的意见》,指出在确保电子处方来源真实可靠的前提下,允许网络销售除国家实行特殊管理的药品以外的处方药。
2.交通运输部、公安部、国家卫生健康委、中国民用航空局、国家药品监督管理局、中国国家铁路集团有限公司六部门联合印发通知,就进一步做好新冠病毒疫苗货物运输组织和服务保障工作进行部署。
3.财政部发布《医药企业会计信息质量检查公告》,对19家医药企业作出行政处罚,涉及江苏恒瑞、华润三九、礼来等。19家医药企业存在的问题主要有三个方面:使用虚假发票、票据套取资金体外使用;虚构业务事项或利用医药推广公司套取资金;账簿设置不规范等。
4.国家卫生健康委、国家市场监管总局、国家医保局、国家中医药局、国家药监局、中央军委后勤保障部卫生局联合发布《不合理医疗检查专项治理行动工作方案》,对行动目标、行动范围、重点内容、责任分工、实施步骤和工作要求等方面进行了规定。专项治理活动时间为2021年4月至2022年3月。
5.国家药监局发布《2021年国家医疗器械抽检产品检验方案》的通知,要求各省、自治区、直辖市药品监督管理局及新疆生产建设兵团药品监督管理局、中国食品药品检定研究院应按照检验方案组织相关检验机构按医疗器械强制性标准以及经注册或者备案的产品技术要求(注册产品标准)开展检验工作。
6.国家药监局发布《国家医疗器械质量抽查检验工作程序》,规范国家医疗器械质量抽查检验工作。
7.国家药监局发布《国家医疗器械监督抽检结果的通告(第2号)(2021年第25号)》,对电动轮椅车、软性接触镜、一次性使用鼻氧管等9个品种进行了产品质量监督抽检,共55批(台)产品不符合标准规定。
8.国家药监局发布《基于同类治疗药物的肿瘤伴随诊断试剂说明书更新与技术审查指导原则》《实时荧光PCR分析仪注册技术审查指导原则》《轮状病毒抗原检测试剂注册技术审查指导原则》《B群链球菌核酸检测试剂注册技术审查指导原则》和《人细小病毒B19 IgM/IgG抗体检测试剂注册技术指导原则》5项注册技术审查指导原则。
9.国家药监局发布公告,桂附地黄颗粒由处方药转化为非处方药,并发布品种名单及非处方药说明书范本。
10.国家药监局注销Allergan公司的硅凝胶填充乳房植入体、长春白求恩医疗器械有限公司的一次性使用精密过滤输液器带针和徐州一佳医疗器械有限公司的一次性使用输液器带针3个医疗器械注册证书。
11.国家药监局对曲马多栓剂和复方制剂的药品说明书进行修订,对其增加警示语,修订【不良反应】【禁忌】【注意事项】【孕妇及哺乳期妇女用药】【儿童用药】【老年用药】【药物相互作用】项。
12. CDE发布《用于产生真实世界证据的真实世界数据指导原则(试行)》,指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发。
13.CDE组织起草了《盐酸乐卡地平片生物等效性研究技术指导原则(征求意见稿)》《盐酸厄洛替尼片生物等效性研究技术指导原则(征求意见稿)》等16个生物等效性研究技术指导原则征求意见稿,征求意见截止时间为5月12日。
14.CDE就《儿童用化学药品改良型新药临床试验技术指导原则(征求意见稿)》公开征求意见,征求意见截止时间为5月13日。
15.CDE发布《化学仿制药参比制剂目录(第四十二批)》,涉及依折麦布辛伐他汀片等药品。
16.国家药典委发布《关于实行〈中国药典〉药包材标准品种监护人管理的通知》,以确保相关标准的正确执行和持续改进。
产品研发 · 上市信息
1.国家药监局批准深圳睿心智能医疗科技有限公司生产的创新产品“冠状动脉CT血流储备分数计算软件”的注册申请。该产品基于冠状CT血管影像计算获得CT血流储备分数,在进行冠状血管造影检查之前,辅助培训合格的医技人员评估稳定性冠心病患者的功能性心肌缺血症状。
2.国家药监局发布4期药品批准证明文件待领信息,共包括182个受理号,涉及上海君实生物医药科技股份有限公司等企业。(截至4月18日)

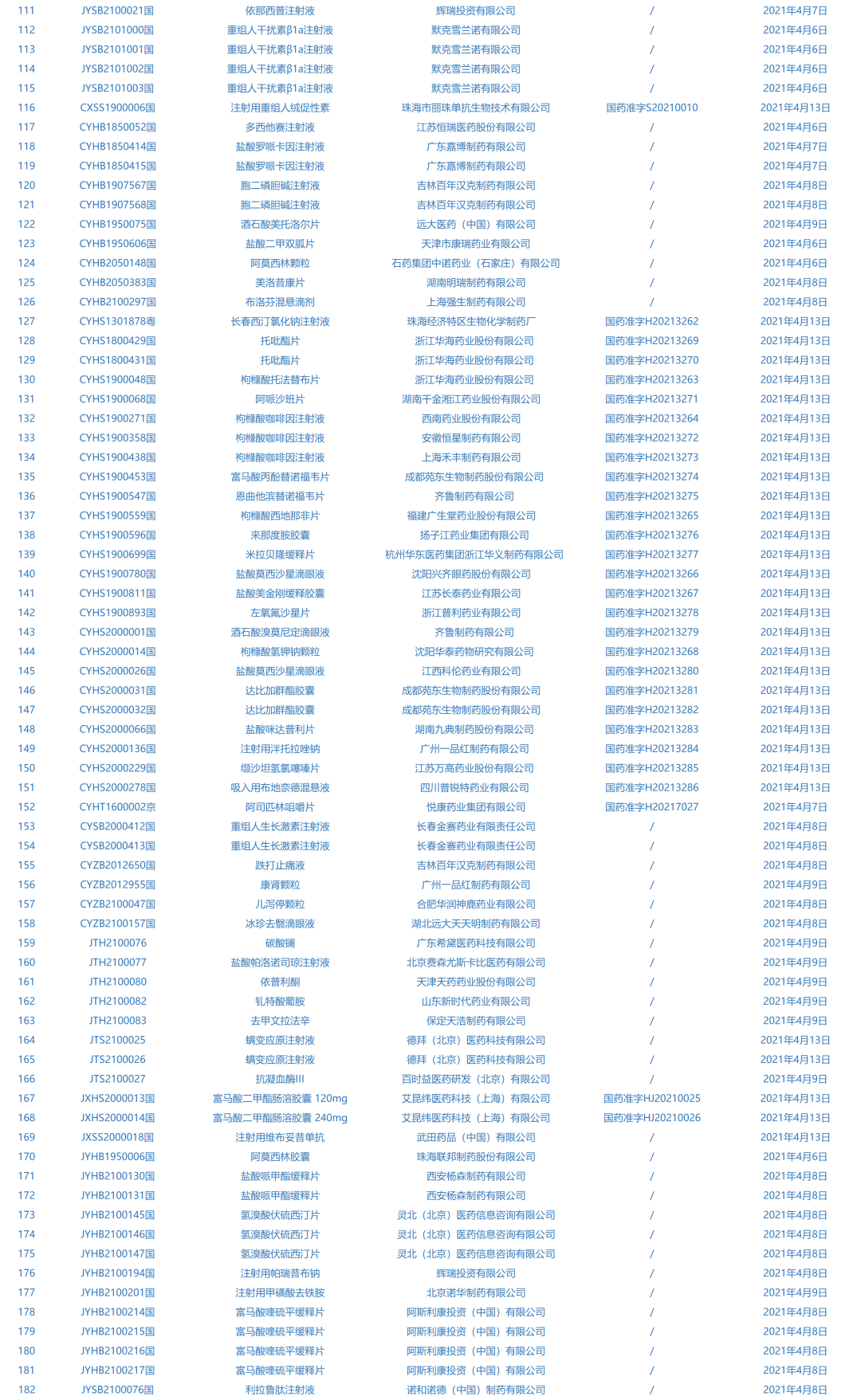
3.国家药监局发布5期医疗器械批准证明文件(准产)待领信息,共包括105个受理号,涉及赛诺医疗科学技术股份有限公司等企业。(截至4月18日)

4.CDE网站公示14个仿制药一致性评价任务,涉及盐酸伐昔洛韦片等药品。(截至4月18日)
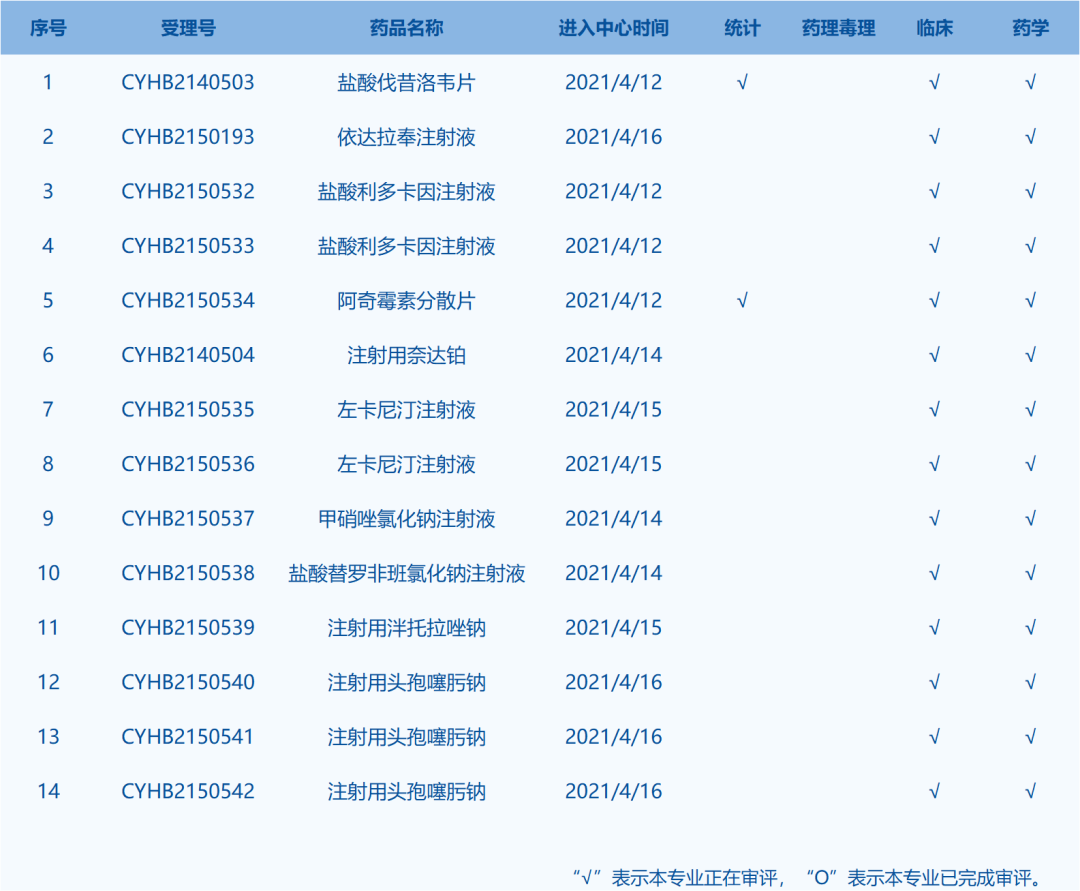
5.CDE承办受理23个新药上市申请,包括散风通窍滴丸等药品。(截至4月18日)

6.国家药监局器审中心公示医疗器械优先审批申请审核结果,上海联影医疗科技股份有限公司的X射线计算机体层摄影设备因属于列入国家重点研发计划的医疗器械,符合优先审批情形,拟定予以优先审批。
医药企业观察
1.默沙东宣布终止免疫调节剂MK-7110(此前称作CD24Fc)治疗COVID-19项目的进一步开发;终止口服抗病毒药物molnupiravir(EIDD-2801/MK-4482)在重症住院患者中的II/III期研究,继续推进molnupiravir在门诊轻中度患者中的III期研究。
2.赛神医药宣布与礼来签订了独家许可协议,于大中华地区(包括中国大陆、香港、澳门和台湾地区)开发和商业化礼来的一种被称为“α-突触核蛋白”(α-synuclein)的靶向疗法。
3.索元生物与Rumpus Therapeutics/Aytu Biopharma签订了开发DB102(enzastaurin)用于治疗血管性埃勒斯-当洛综合征(vEDS)等罕见遗传病的全球授权协议。根据协议,Aytu BioPharma将负责DB102针对这一罕见病的临床开发及商业化,并将支付索元生物1亿美元的里程碑及销售提成。(注:Aytu Biopharma已正式收购Rumpus Therapeutics )
4.上交所披露受理益方生物科技(上海)股份有限公司科创板IPO申请,该公司拟在科创板募资24.09亿元,由中信证券担任保荐机构。
5.成都海博为药业完成数千万元A轮融资,本轮融资由怀格资本领投,川发展旗下四川院士科技创新基金等投资人跟投。本轮融资将用于该公司多个1类新药项目研发以及今明两年将完成的四个IND申报项目的推进。
6.诺洁贝生物完成3000万美元A轮融资,本轮融资由翼朴资本领投,苇渡资本以及老股东北极光创投、元生创投跟投。此轮融资主要用于诺洁贝生物多款基因治疗管线的临床产品的准备和cGMP生产车间的建设。
7.药兜网完成数亿元C轮融资,本轮融资由摩根士丹利领投、老股东南曦创投继续追加投资。“互联网+医疗健康”成资本焦点。
8.昊海生科发布公告称,控股子公司河南赛美视生物科技有限公司的可折叠、疏水丙烯酸酯、非球面、散光人工晶状体产品获欧盟CE认证证书。
9. 方盛制药拟以人民币1460万元受让控股子公司三花制药持有的药品“三花接骨散”的所有权(包括但不限于该品种的研制原始资料、药品处方、生产工艺和质量标准、再注册资料及新药证书等生产技术和知识产权)。
10.博济医药拟以自有资金4842万元收购深圳市华融盛科技有限公司持有的博济医药子公司香港永禾科技有限公司44%股权,本次交易前,博济医药持有香港永禾51%的股权,本次交易完成后,博济医药将持有香港永禾95%的股权。
药械集中采购
1.新疆维吾尔自治区医保局就《新疆维吾尔自治区 新疆生产建设兵团“2+4”联盟组织药品集中带量采购和使用工作实施方案(征求意见稿)》公开征求意见。由新疆维吾尔自治区、新疆生产建设兵团发起,联合陕西、甘肃、青海、宁夏等省区的医疗机构组成的联盟(“2+4”联盟)正式亮相,将常态化制度化开展药品集中带量采购。
2.浙江省医保局发布《关于完善药品集中采购平台准入机制的通知》,明确短缺药、医保基药品种、生物制品、儿科用药等7类药品准入机制。
3.浙江省药械采购中心发布通报称,哈尔滨誉衡制药有限公司的鹿瓜多肽注射液在浙江省存在商业贿赂行为,将该企业在浙江省医药价格和招采失信等级评为“严重”,并暂停该企业鹿瓜多肽注射液在线交易。
4.京津冀医药联合采购平台发布《京津冀“3+N”联盟药品联合带量采购项目拟中选结果公示》,共有10个品种产生拟中选结果,涉及20个品规。
文章来源:中国医药报


